= 他サイトのコンテンツで表示される画像から =
 固体(solid) |
 液体(liquid) |
|---|---|
 気体(gas) | |
 固体(solid) |
 液体(liquid) |
|---|---|
 気体(gas) | |
物質を構成する分子・原子などの粒子は個々に微視的な運動をしており,その運動の激しさを平均したものが実は物質の温度なのです。その運動が完全に止まっている状態を絶対零度(0K,-273.15℃)といい(もっと厳密な定義がありますが),それより低い温度はあり得ないことになります。さらに,物質のないところでは“温度”という概念は成り立たなくなります。
また,粒子と粒子の間には引力が働いています。分子と分子の間の引力は分子間力です。この引力と上の運動の激しさの兼ね合いでその物質の状態が決まります。
運動によるバラバラになろうとする力が小さい間は引力のほうが勝って固体状態になりますが,運動が激しくなるにしたがって(温度が上がるにしたがって)液体,気体へと変化するのです。
詳しくはアニメを作成させていただいた以下のページの解説の参考にしてください。
※上のアニメ画像は,「のりさんのパソコン物理」のJavaアプレット『分子ビリヤードで遊ぼう(気体,液体,固体って何?)』によるシミュレーション画面を,動画キャプチャ(使用したフリーウェア)で切り取って作成したものです。原作Javaアプレット版とは異なり,アニメは同じ場面の繰り返しになってることにご注意ください。
アニメ画像の転載をご承諾くださった原作者に感謝いたします。
また,以下のページも大変わかりやすく,参考になります。
- 『物質の三態・1』,『同・2』(山村女子高等学校・吉野先生他による「楽しい高校化学」収録)
- 『Web教材 水の状態変化』(「岐阜大学教育学部・理科教育講座地学教室/理科教育用教材データベース」収録) …分子動力学法シミュレーション
- 『分子間力を及ぼし合う粒子系』(東海大学開発工学部・松浦研究室による「初歩の物理のページ」収録)
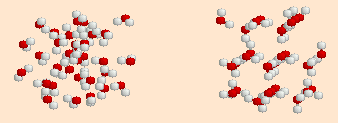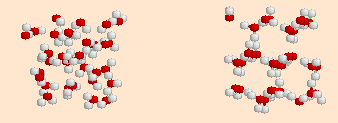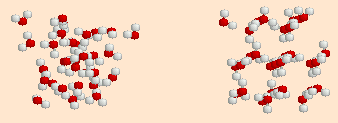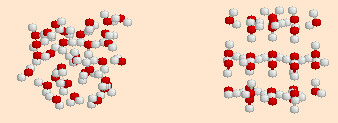
物質の密度は同一の体積の中にどれだけの重さの粒子がどれだけ詰まっているかで決まります。通常,物質は液体よりも固体の方が密度が大きいですが,水は液体状態の3.98℃で密度が最大になるという不思議な物質です。だから水に氷が浮かぶのですね。またこの性質はいろいろな現象にとても重要な役割を果たしています。
その秘密が上のアニメになります。固体は整然とした結晶構造をとっており,これが雪の結晶の形にも関係しているのです。液体の方は一見無秩序な構造ですが,とてもうまい具合に並んでいて同一体積には固体の場合よりたくさん詰め込まれているのです。
以下のオリジナルデータのページで,それぞれの構造を拡大して回転して見ると,液体の方が固体にある定まった形の空隙が無くて,密に詰まっていることが実感できるでしょう。
※アニメ画像は,“Chemistry 101/UNDERSTANDING DRUGS(Department of Chemistry, Wellesley College )”内の分子表示プラグインChime等を駆使した化学教材集の中にある“WATER & SOLUBILITIES”の表示画像を,動画キャプチャで切り取って作成したものです。