→ Jmol版 ←
|
|
α-アミノ酸の基本構造
《中心炭素に,水素・アミノ基(−NH2)・カルボキシル基(-COOH)と特有の置換基が結合している》
アミノ酸のいろいろな情報を表示させてみよう(初期表示ははアラニン)
|
《参考》 |
→ Chimeマニュアル参照
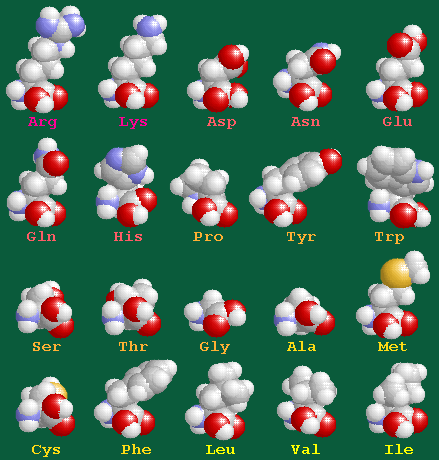
※hydropathy index順に示したアミノ酸(上段の左から右へ昇順) → 生体分子と水素結合
※構成元素は,H,C,N,O,S の5種類
※参考:秀丸マクロamino_bcaa.mac(BCAAのIle・Val・LeuおよびCysの区別とカウント)
アミノ酸および特性基の親水性・疎水性
→ 簡略版(有機性・無気性値除く) | PDB部分データリスト/別版 ←
| アミノ酸 | 分子式 | CAS RN | hydropathy index |
O | I | I/O | 特性基 R | log P | 酸性・塩基性 | 極性・非極性 | 等電点 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| O' | I' | I'/O' | |||||||||||||
| Asn | N | アスパラギン | H2NCOCH2CH(NH2)COOH | 70-47-3 | -3.5 | 80 | 420 | 5.250 | 40 | 200 | 5.000 | -3.82 | 中性 | 極性(中性) | 5.41 |
| Ser | S | セリン | HOCH2CH(NH2)COOH | 56-45-1 | -0.8 | 60 | 320 | 5.333 | 20 | 100 | 5.000 | -3.07 | 中性 | 極性(中性) | 5.68 |
| Asp | D | アスパラギン酸 | HOOCCH2CH(NH2)COOH | 56-84-8 | -3.5 | 80 | 370 | 4.625 | 40 | 150 | 3.750 | -3.89 | 酸性 | 極性(酸性) | 2.77 |
| Gln | Q | グルタミン | H2NCO-CH2CH2CH(NH2)COOH | 56-85-9 | -3.5 | 100 | 420 | 4.200 | 60 | 200 | 3.333 | -3.64 | 中性 | 極性(中性) | 5.65 |
| Glu | E | グルタミン酸 | HOOCCH2CH2CH(NH2)COOH | 56-86-0 | -3.5 | 100 | 370 | 3.700 | 60 | 150 | 2.500 | -3.69 | 酸性 | 極性(酸性) | 3.22 |
| Thr | T | トレオニン | CH3CH(OH)CH(NH2)COOH | 72-19-5 | -0.7 | 80 | 320 | 4.000 | 40 | 100 | 2.500 | -2.94 | 中性 | 極性(中性) | 6.16 |
| Arg | R | アルギニン | H2N(=NH)NHC3H6CCH(NH2)COOH | 74-79-3 | -4.5 | 120 | 410 | 3.417 | 80 | 190 | 2.375 | -4.20 | 塩基性 | 極性(塩基性) | 10.76 |
| His | H | ヒスチジン | H2NCH[CH2(C3H3N2)]COOH | 71-00-1 | -3.2 | 120 | 372 | 3.100 | 80 | 152 | 1.900 | -3.32 | 塩基性 | 極性(塩基性) | 7.59 |
| Gly | G | グリシン | H2NCH2COOH | 56-40-6 | -0.4 | 40 | 220 | 5.500 | 0 | 0 | − | -3.21 | 中性 | 非極性(疎水性) | 5.97 |
| Lys | K | リシン | H2N(CH2)4CH(NH2)COOH | 56-87-1 | -3.9 | 120 | 290 | 2.417 | 80 | 70 | 0.875 | -3.05 | 塩基性 | 極性(塩基性) | 9.74 |
| Tyr | Y | チロシン | HO(C6H4)CH2CH(NH2)COOH | 60-18-4 | -1.3 | 180 | 335 | 1.861 | 140 | 115 | 0.821 | -2.26 | 中性 | 極性(中性) | 5.66 |
| Trp | W | トリプトファン | (C8H6N)-CH2CH(NH2)COOH | 73-22-3 | -0.9 | 220 | 350 | 1.591 | 180 | 130 | 0.722 | -1.05 | 中性 | 非極性(疎水性) | 5.89 |
| Cys | C | システイン | HSCH2CH(NH2)COOH | 52-90-4 | 2.5 | 100 | 240 | 2.400 | 60 | 20 | 0.333 | -2.49 | 中性 | 極性(中性) | 5.07 |
| Met | M | メチオニン | CH3SCH2CH2CH(NH2)COOH | 63-68-3 | 1.9 | 140 | 240 | 1.714 | 100 | 20 | 0.200 | -1.87 | 中性 | 非極性(疎水性) | 5.74 |
| Pro | P | プロリン | (C4H8N)-COOH | 147-85-3 | -1.6 | 100 | 230 | 2.300 | 60 | 10 | 0.167 | -2.54 | 中性 | 非極性(疎水性) | 6.30 |
| Phe | F | フェニルアラニン | (C6H5)CH2CH(NH2)COOH | 63-91-2 | 2.8 | 180 | 235 | 1.306 | 140 | 15 | 0.107 | -1.38 | 中性 | 非極性(疎水性) | 5.48 |
| Ala | A | アラニン | CH3CH(NH2)COOH | 56-41-7 | 1.8 | 60 | 220 | 3.667 | 20 | 0 | 0 | -2.85 | 中性 | 非極性(疎水性) | 6.00 |
| Val | V | バリン | (CH3)2CHCH(NH2)COOH | 72-18-4 | 4.2 | 90 | 220 | 2.444 | 50 | 0 | 0 | -2.26 | 中性 | 非極性(疎水性) | 5.96 |
| Leu | L | ロイシン | (CH3)2CHCH2CH(NH2)COOH | 61-90-5 | 3.8 | 110 | 220 | 2.000 | 70 | 0 | 0 | -1.52 | 中性 | 非極性(疎水性) | 5.98 |
| Ile | I | イソロイシン | C2H5CH(CH3)CH(NH2)COOH | 73-32-5 | 4.5 | 120 | 220 | 1.833 | 80 | 0 | 0 | -1.70 | 中性 | 非極性(疎水性) | 6.02 |
※log PはOn-Line Log P Calculation掲載の実験値
※極性・非極性はChimeのProtein選択様式と関連(参考ページ)
《参考》分子と分子の相互作用(QSARと有機概念図から)〔特性基RのI・O値を用いた計算例:1ereのSITE表示と有機概念図計算〕
《参考》1文字アミノ酸配列から各種HTMLデータを作成する秀丸マクロ
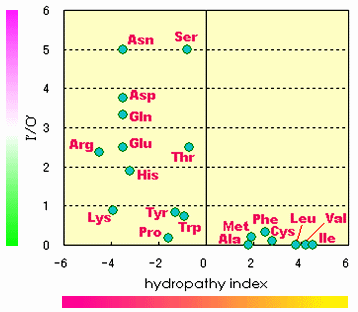
図1 アミノ酸残基のhydropathy indexとI'/O'値の比較(Glyを除く)
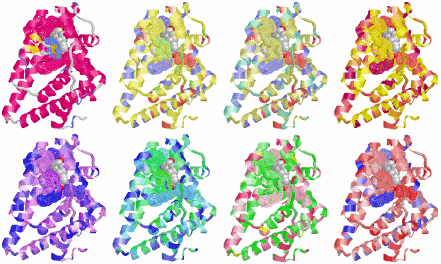
図2(拡大) アミノ酸または残基の親水性・疎水性による色分け(1ereのChain A).
《上》左から,二次構造,酸性・中性〈芳香族〉・塩基性アミノ酸区別,極性・非極性区別,hydropathy index順表示.
《下》左から,log P値順, 有機概念図I/O値順(アミノ酸),同(特性基 R),等電点順表示.
※PDBコード順データリスト,PDBデータのLigand結合部位で各表示可能.
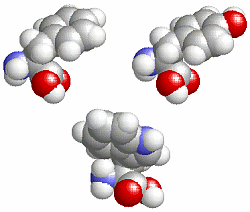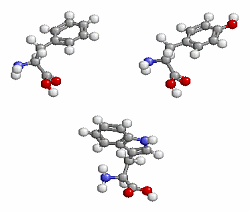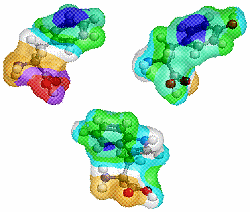
図3 芳香族アミノ酸(Phe,Tyr,Trp);図2の塩基性アミノ酸区別,極性・非極性区別表示では黄緑色で表示される.
※参考雑誌記事:青木康展,『ベンゼンはなぜ動物には有害か ─毒性研究を広く自然界を見渡して考える』,科学,2007年9月号,pp.986-989
…p.987の「動物のフェニル基は植物に依存している」に関連して(Jmol版では親油ポテンシャル表示不可);関連資料
旧資料 有機概念図I/O値順(アミノ酸)に示したアミノ酸
※以下の分子モデル上でクリックすると,別窓にChime版分子が表示されます
→ 分子と分子の相互作用(QSARと有機概念図から) | PDB部分データリスト ←
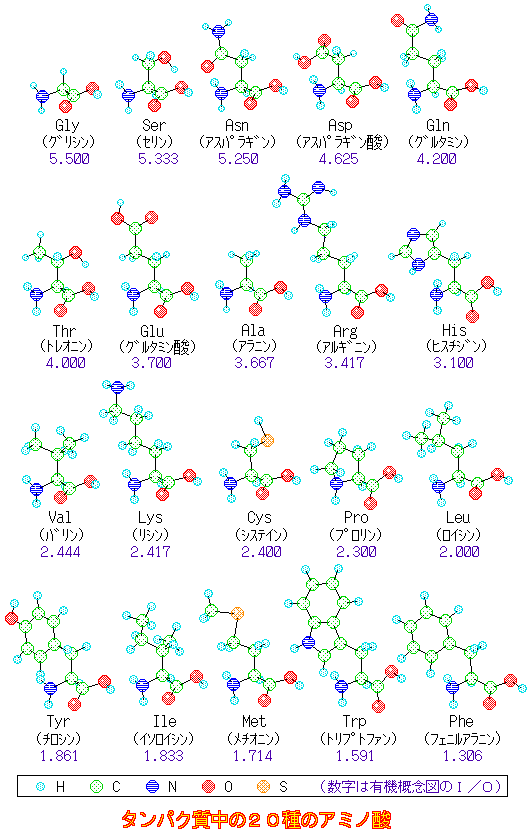
※有機概念図について 『Excel97用有機概念図計算シート』の使用方法 | アミノ酸とDNA塩基の有機性・無機性(画像)