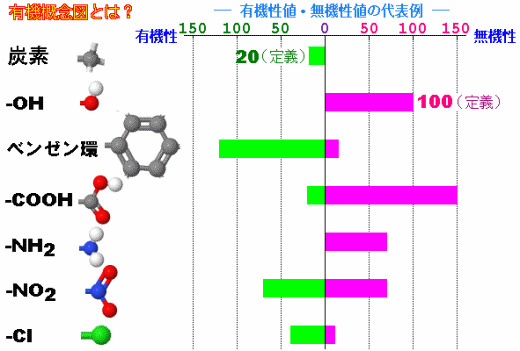
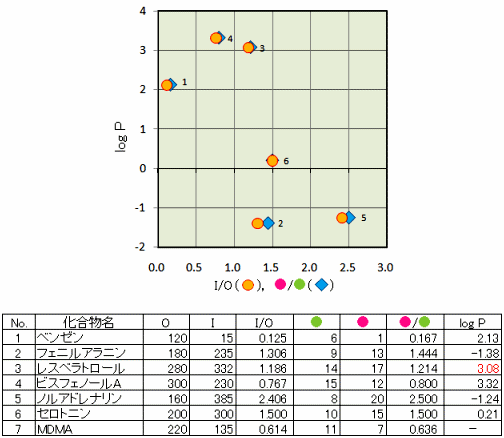
有機概念図簡易計算機(タンパク質)
★2色のレゴブロックなどであらかじめ各アミノ酸の●の個数だけ色別に接着して残基名をつけておき,それらをつなぐとよい。
| アミノ酸 |
特性基 R |
概数(20を基準) |
概数(●=20)
※複数ある場合の繰り上がり・繰り下がりは無視 |
O
(油) |
I
(水) |
I/O |
油 |
水 |
油 |
水 |
| Ile |
イソロイシン |
 |
80 |
0 |
0 |
4 |
0 |
●●●● |
|
| Leu |
ロイシン |
 |
70 |
0 |
0 |
4 |
0 |
●●●● |
|
| Val |
バリン |
 |
50 |
0 |
0 |
3 |
0 |
●●● |
|
| Ala |
アラニン |
 |
20 |
0 |
0 |
1 |
0 |
● |
|
| Phe |
フェニルアラニン |
 |
140 |
15 |
0.107 |
7 |
1 |
●●●●●●● |
● |
| Pro |
プロリン |
 |
60 |
10 |
0.167 |
3 |
1 |
●●● |
● |
| Met |
メチオニン |
 |
100 |
20 |
0.200 |
5 |
1 |
●●●●● |
● |
| Cys |
システイン |
 |
60 |
20 |
0.333 |
3 |
1 |
●●● |
● |
| Trp |
トリプトファン |
 |
180 |
130 |
0.722 |
9 |
7 |
●●●●●●●●● |
●●●●●●● |
| Tyr |
チロシン |
 |
140 |
115 |
0.821 |
7 |
6 |
●●●●●●● |
●●●●●● |
| Lys |
リシン |
 |
80 |
70 |
0.875 |
4 |
4 |
●●●● |
●●●● |
| Gly |
グリシン |
 |
0 |
0 |
− |
0 |
0 |
|
|
| His |
ヒスチジン |
 |
80 |
152 |
1.900 |
4 |
8 |
●●●● |
●●●●●●●● |
| Arg |
アルギニン |
 |
80 |
190 |
2.375 |
4 |
10 |
●●●● |
●●●●●●●●●● |
| Thr |
トレオニン |
 |
40 |
100 |
2.500 |
2 |
5 |
●● |
●●●●● |
| Glu |
グルタミン酸 |
 |
60 |
150 |
2.500 |
3 |
8 |
●●● |
●●●●●●●● |
| Gln |
グルタミン |
 |
60 |
200 |
3.333 |
3 |
10 |
●●● |
●●●●●●●●●● |
| Asp |
アスパラギン酸 |
 |
40 |
150 |
3.750 |
2 |
8 |
●● |
●●●●●●●● |
| Ser |
セリン |
 |
20 |
100 |
5.000 |
1 |
5 |
● |
●●●●● |
| Asn |
アスパラギン |
 |
40 |
200 |
5.000 |
2 |
10 |
●● |
●●●●●●●●●● |
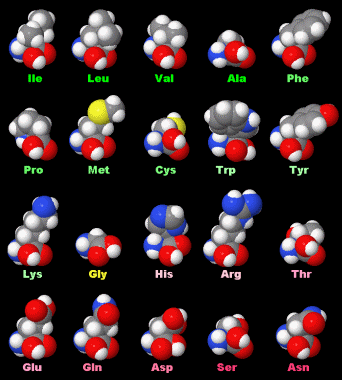

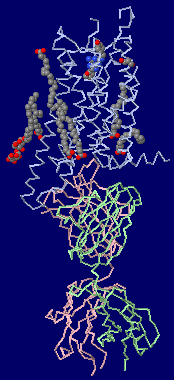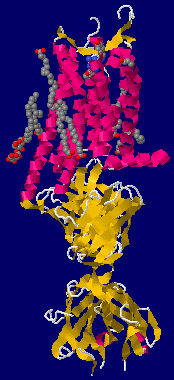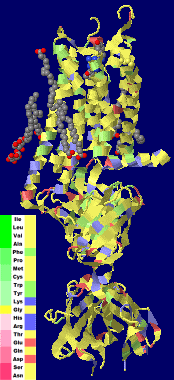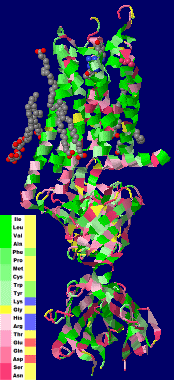
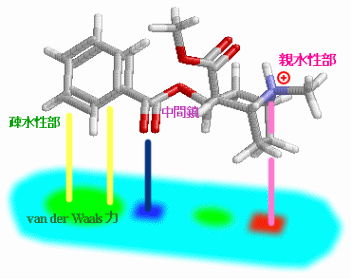
〔中〕赤と緑で“水と油”;身近なものによる分層教材の例(Log Pをポケットに!参照;右の図はクリックで関連ページへ)
上層:緑色のマーカーでプラシート上に厚く塗り乾いてからオクタノールまたはサラダオイルで溶かして。
下層:温湯に食紅を溶かして。
※上層をサラダオイルにしたものを用いて公民館サイエンスカフェ『生命を支える美しい分子たち』(2012/03/03)で話をしました。
参考:アミノ酸および特性基の親水性・疎水性
| アミノ酸 |
hydropathy
index |
特性基 R |
log P |
酸性・塩基性 |
極性・非極性 |
Cleftの分類 |
等電点 |
| O |
I |
I/O |
| Ile |
I |
イソロイシン |
4.5 |
80 |
0 |
0 |
-1.70 |
中性 |
非極性(疎水性) |
Aliphatic |
6.02 |
| Leu |
L |
ロイシン |
3.8 |
70 |
0 |
0 |
-1.52 |
中性 |
非極性(疎水性) |
Aliphatic |
5.98 |
| Val |
V |
バリン |
4.2 |
50 |
0 |
0 |
-2.26 |
中性 |
非極性(疎水性) |
Aliphatic |
5.96 |
| Ala |
A |
アラニン |
1.8 |
20 |
0 |
0 |
-2.85 |
中性 |
非極性(疎水性) |
Aliphatic |
6.00 |
| Phe |
F |
フェニルアラニン |
2.8 |
140 |
15 |
0.107 |
-1.38 |
中性 |
非極性(疎水性) |
Aromatic |
5.48 |
| Pro |
P |
プロリン |
-1.6 |
60 |
10 |
0.167 |
-2.54 |
中性 |
非極性(疎水性) |
Pro & Gly |
6.30 |
| Met |
M |
メチオニン |
1.9 |
100 |
20 |
0.200 |
-1.87 |
中性 |
非極性(疎水性) |
Aliphatic |
5.74 |
| Cys |
C |
システイン |
2.5 |
60 |
20 |
0.333 |
-2.49 |
中性 |
極性(中性) |
Cysteine |
5.07 |
| Trp |
W |
トリプトファン |
-0.9 |
180 |
130 |
0.722 |
-1.05 |
中性 |
非極性(疎水性) |
Aromatic |
5.89 |
| Tyr |
Y |
チロシン |
-1.3 |
140 |
115 |
0.821 |
-2.26 |
中性 |
極性(中性) |
Aromatic |
5.66 |
| Lys |
K |
リシン |
-3.9 |
80 |
70 |
0.875 |
-3.05 |
塩基性 |
極性(塩基性) |
Positive |
9.74 |
| Gly |
G |
グリシン |
-0.4 |
0 |
0 |
− |
-3.21 |
中性 |
非極性(疎水性) |
Pro & Gly |
5.97 |
| His |
H |
ヒスチジン |
-3.2 |
80 |
152 |
1.900 |
-3.32 |
塩基性 |
極性(塩基性) |
Positive |
7.59 |
| Arg |
R |
アルギニン |
-4.5 |
80 |
190 |
2.375 |
-4.20 |
塩基性 |
極性(塩基性) |
Positive |
10.76 |
| Thr |
T |
トレオニン |
-0.7 |
40 |
100 |
2.500 |
-2.94 |
中性 |
極性(中性) |
Neutral |
6.16 |
| Glu |
E |
グルタミン酸 |
-3.5 |
60 |
150 |
2.500 |
-3.69 |
酸性 |
極性(酸性) |
Negative |
3.22 |
| Gln |
Q |
グルタミン |
-3.5 |
60 |
200 |
3.333 |
-3.64 |
中性 |
極性(中性) |
Neutral |
5.65 |
| Asp |
D |
アスパラギン酸 |
-3.5 |
40 |
150 |
3.750 |
-3.89 |
酸性 |
極性(酸性) |
Negative |
2.77 |
| Ser |
S |
セリン |
-0.8 |
20 |
100 |
5.000 |
-3.07 |
中性 |
極性(中性) |
Neutral |
5.68 |
| Asn |
N |
アスパラギン |
-3.5 |
40 |
200 |
5.000 |
-3.82 |
中性 |
極性(中性) |
Neutral |
5.41 |
※hydropathy indexは以下を参照;Kyte and Doolittle, J. Mol. Biol., 157, 105-132(1982)
※log PはOn-Line Log P Calculation掲載の実験値
※極性・非極性はChimeのProtein選択様式と関連(参考ページ)
《参考》1文字アミノ酸配列から各種HTMLデータを作成する秀丸マクロ
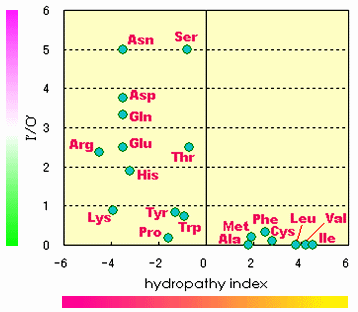
アミノ酸残基の疎水性インデックスとI'/O'値の比較(Glyを除く)
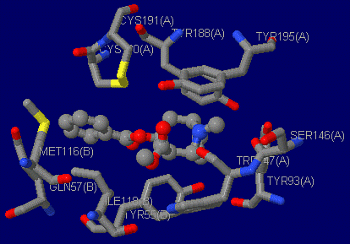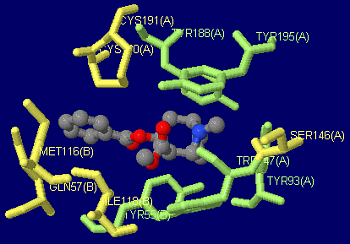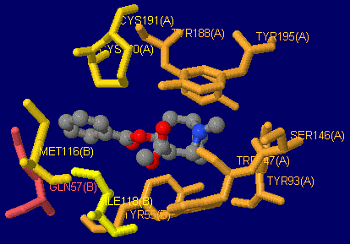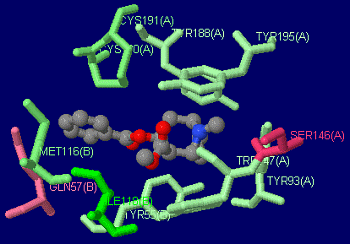
Cleft analysisによるアミノ酸分類(データ例:2hkk)
|
Positive
|
Negative
|
Neutral
|
Aliphatic
|
Aromatic
|
Pro & Gly
|
Cysteine
|
|
H,K,R
|
D,E
|
S,T,N,Q
|
A,V,L,I,M
|
F,Y,W
|
P,G
|
C
|
 パソコンやiPad・iPhoneで使える有機概念図簡易計算アプリを相馬 稔さん(プロジェクトCANI,新潟高度情報専門学校)に開発していただいて公開しました。
パソコンやiPad・iPhoneで使える有機概念図簡易計算アプリを相馬 稔さん(プロジェクトCANI,新潟高度情報専門学校)に開発していただいて公開しました。