【参考Webサイト・文献】 ↑top
- MDL,Chime
- Protein Data Bank;国内ミラーはPDBj
- 本間善夫・川端潤,「パソコンで見る動く分子事典」,講談社ブルーバックス(1999)
- 本間善夫,『分子モデル可視化ツールChimeを使った化学教育』,理科教室,2005年6月号,星の環会
- 本間善夫,『インターネットによる知の共有の試み』,化学,2000年5月号,化学同人
- 本間善夫・吉田弘・松浦博厚,『分子表示プラグインを利用した分子振動アニメーション』,化学ソフトウェア学会年会2001研究討論会講演要旨集,pp.90-91;分子振動データ集
- 本間善夫,『Webブラウザを利用した重ね合わせ分子データによる教材の作成』,日本化学会第81春季年会(2002年)講演要旨集I,p.650;複合分子と分子の重ね合わせ/分子データの作成方法
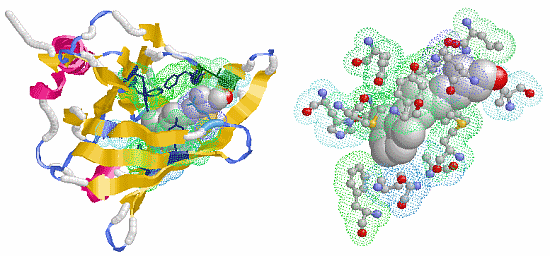
- 本間善夫,『PDBデータのLigand結合部位のデータ集作成』,日本コンピュータ化学会2003秋季年会講演要旨集,pp.84-85;PDBデータのLigand結合部位
- 本間善夫,『生体関連分子学習のためのWeb教材の作成』,ナノ学会第3回大会講演予稿集(2005),p.138
- 本間善夫,『2004年のWeb情報発信から ―鳥インフルエンザ,抗生物質,水俣病,P450―』,科学技術社会論学会第3回年次研究大会予稿集,pp.23-24
- 吉田弘,分子モデリングプログラム MOLDA
- 千田範夫,分子計算支援システム Winmostar ※参考:port:3016 feat.Winmostar
- 伊東章,化学工学資料のページ
- 科学技術振興機構,Webラーニングプラザ(技術者Web学習システム)
- 文部科学省,「平成15年度 科学技術の振興に関する年次報告」
- 科学技術振興機構,理科ねっとわーく ★
- 分子科学研究所 編,「分子科学者がいどむ12の謎」,化学同人(2005)
- 時実象一,「理系のためのインターネット検索術」,講談社ブルーバックス(2005) ※参考:検索サイトリンク集
- Chimeを活用するために
- Chime解説サイト例
- 速報コンテンツ例 ※参考(情報の国際競争):Googleによる“KU-55933”検索結果,同“温室 SF5CF3”検索結果
- 推奨ツール例

【デモンストレーションに向けて】 ↑top
【2005年度のレポートを読んで】 ↑top
短い集中講義の中で,Chimeの使い方と分子の見方,インターネットやPCの利用方法など,盛り沢山に話したこともあって,説明不十分なところもあったと思いますが,『Chimeデータ集の中から低分子・生体高分子をそれぞれ1つずつ選んで画像とともに説明を加える』という課題に取り組んでもらいました。以下に全体的な感想を列挙しますので,今後の参考にしてもらえたらと思います。他の教科のレポートとも共通する部分も多いでしょう。
- レポートである以上,オリジナリティを大切に。いくつかの文献やWeb情報,過去の講義(中学・高校時代を含めて)で習ったことも踏まえて,比較したり批判することも重要です。
- 例えば今回のレポートでは,なぜぞの分子を取り上げたのかや,商品や過去の実験等でその分子と接したことがある場合はそのことにも触れるとよかったと思います。生体分子の場合は多くの場合,自分自身のことでもあるのですから。講義で紹介した広島大学・吉田先生の分子モデリングプログラムMOLDAページにある『私たちは分子でできている』をもう一度読んでもらえたら幸いです。
- 「引用部分」と「自分の文章」の区別は明確に。これは書籍や論文誌でも守られているはずです。
※少し畑違いの分野の文章ですが,引用部分の文字色を変えるなどした以下を少し参考にしてください。 → 生命を考える家庭科
- 上記例文にあるように,引用文献やWeb情報は作者や作成年がわかるようにする必要があり,その部分をどこから引用したかわかるようにする必要があります。文献の書き方は,雑誌によって多少違いますが盛るべき内容は共通です。特に発行年はそれがいつの時点のデータであるかを知る上で不可欠です。Web情報も見た日時を記載するといいでしょう。
- Webページの文章や画像を引用する時は著作権に十分注意する必要があります。
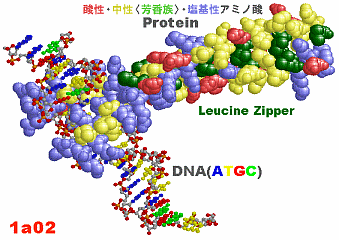
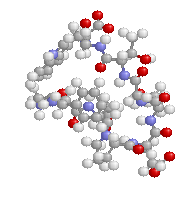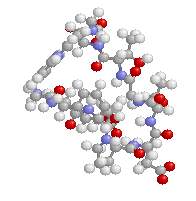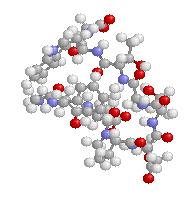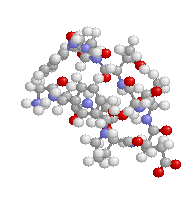
- その意味で,私のページのChime利用コンテンツは,教育用にはフリーにしていますので,いろいろ表示を変えて自分独自の表現にしたものを活用し,分子の見方をわかりやすく説明することは今後の化学の学習でも有用と考えています。今後も分子を3次元で見る意味を考えながら利用して欲しいと思います。例えば,同じDNAの部分構造(14名が取り上げていました)でも以下のようにすることで,文章だけではわかりにくいことが一目瞭然になるでしょう。
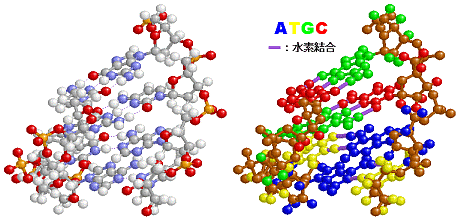
- 文章を引用する場合は,その中の語句や物性単位などでわからないものがあったら,それをきちんと調べて自分の言葉にして表記する必要があります。そうでないと,語句の書き間違いや誤った表現をしかねません。
- Web情報を見る時は,URL(アドレス)などを見て作者の立場など(大学の研究者,公的機関の資料,企業の宣伝,学生のレポートなど,当然書き方も違っています)を知った上で利用する必要があります。
- 上と関連して,何人かが最近情報量の増えているWikipediaの記事を引用していました。これは,ブログと同じようにネット上のツール・システムの1つであるウィキ(wiki)を利用して作られている,ボランティア的な事典で,内容に問題がある場合も少なくありませんし,その利用方法についても同ページに記載されていますので,活用するにはそれなりの注意が必要です。なお,以下の本にはwikiが登場した背景などが書かれています。
- その他,著作権について解説しているWebページがたくさんあるので,きちんと理解しておきましょう。
- 最後になりますが,私自身ネットは情報を受け取る場だけではなく,発信する場だと考えています。講義でブログの話もしましたが,今はその情報発信が本当に簡単になっています。最初にあげた“オリジナリティ”を表出することを意識しながらネットとつき合って欲しいと考えています。
Googleによる情報検索

出張講座のご案内
「生活環境化学の部屋」ホームページ | 「分子の形と性質」学習帳 | iモード化学 | こども省