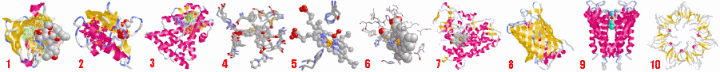2. 原子から生体分子へ ↑TOP
ここで用いる教材はhttp://www.ecosci.jp/bond/hb02.html # に掲載されている。
巨大な生体分子も,原子が集まってできている。その原子は+の電荷を持った陽子と電荷を持たない中性子からなる原子核と,−の電荷を持った電子からできており,原子核と電子は,電磁気力という力で引き合っている。原子が集まって分子ができたり,分子と分子の間で相互作用が生じたりするのも,この電磁気力の働きである。自然界には電磁気力を含めて4種類の力が存在するが,通常の化学や生物では電磁気力だけを考えればよく,これは原子の構造を考えれば当然のことである。
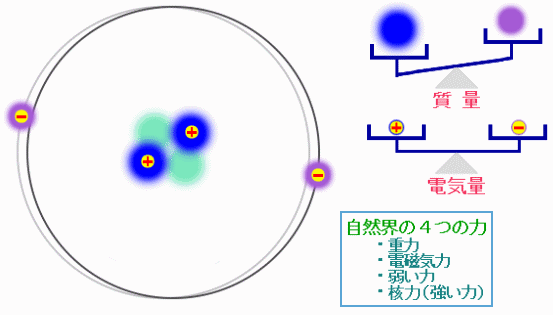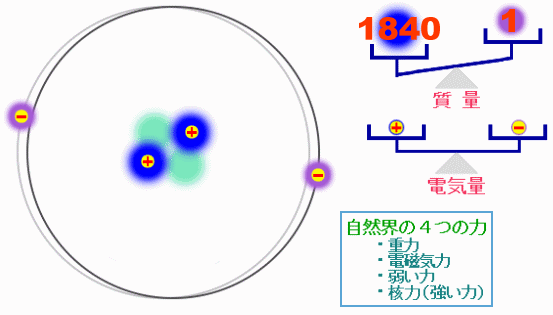
ある原子の構造の模式図と“自然界の4つの力”
※“自然界の4つの力”については以下を参照(高エネルギー加速器研究機構による)
キッズサイエンティスト【自然界の4つの力】*
※参考:平成14年度高等学校教育課程実施状況調査*/科目別分析状況(中間整理)・化学IB*(PDF;問題A2は上と同様の図について)
原子(元素)の種類は陽子数(=電子数)で決まり約100種類あるが,以下に原子番号20までの周期表を電子配置とともに示す。生体分子や身の回りの物質の多くを構成する元素の大部分はこの中に含まれている。

周期表の電気陰性度は結合している原子が電子を引きつける強さの目安であり,これが分子の性質や分子と分子の相互作用を考える上で重要になってくる。
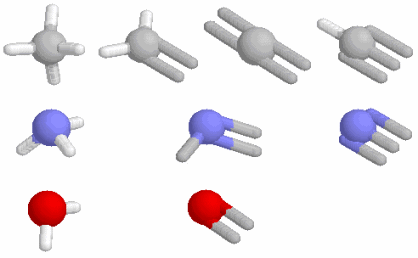
例えば,水分子H2O(折れ線形)は電気陰性度の大きい酸素の側に電子が引きつけられて分子内に電荷のかたよりが生じていて極性分子と呼ばれ,分子は小さいのにお互いの引力が大きいために室温でも液体で存在する。極性の大きい分子は親水性となる。他方,酸素O2のように電荷のかたよりがない分子,二酸化炭素CO2(直線形)やメタンCH4(正四面体形)のようにかたよりがあっても正電荷と負電荷の重心が一致している分子は無極性分子で,疎水性となる。この例のように分子の形(対称性)は分子の性質を決める大きな鍵となっている。
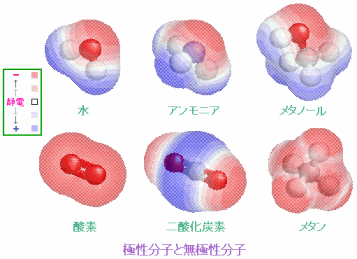
極性分子と無極性分子(http://www.ecosci.jp/chem2/mol_db03.html #);左端は電荷のかたよりを示す静電ポテンシャルの凡例
※分子の形については例えば以下を参照
非結合電子対のドット表示教材 #,酢酸分子の形と軌道 #
Googleイメージ検索『"group theory" molecule』*
Symmetry in Chemistry - Group Theory*(例:ホルムアルデヒド*)
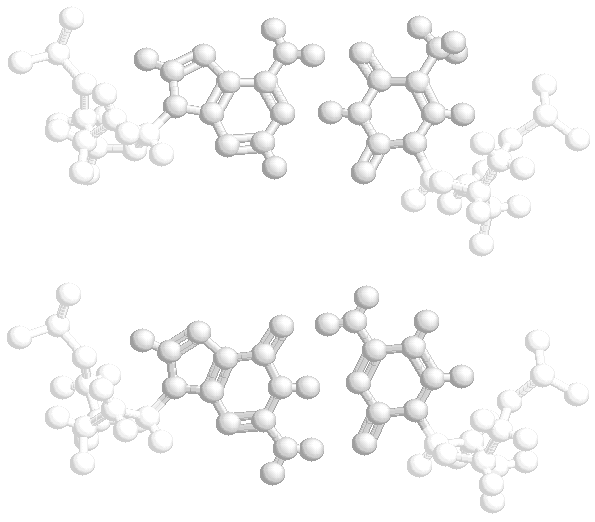
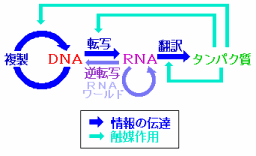
続いてDNAやタンパク質などの生体分子を見てみよう。DNAとRNAはC・H・N・O・Pという5種類の元素だけでできている。一方,タンパク質はC・H・N・O・Sの5種類の元素からなる20種類のアミノ酸(硫黄Sを含むのはこのうち2種類)が長くつながったものが主体となっており,その並ぶ順序を一次構造といい,これを決めているのがDNAなのである。
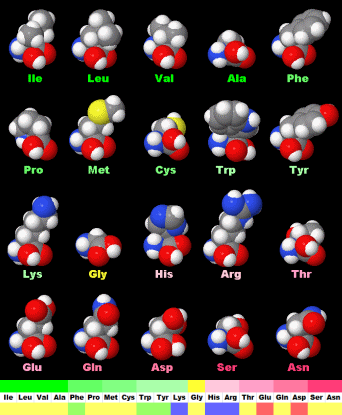
表1の特性基 R のI/O値順に示した20種類のアミノ酸(上段の左から右へ昇順;http://www.ecosci.jp/amino/amino2j.html)
※参考:結合の種類の例(アミノ酸を例に) #
表1 アミノ酸の親水性・疎水性(特性基 R のI/O値順) → タンパク質中の20種類のアミノ酸 ↑TOP
| アミノ酸 |
特性基 R |
hydropathy
index |
極性% |
log P |
酸性・塩基性 |
極性・非極性 |
Cleftの分類 |
等電点 |
| O |
I |
I/O |
| Ile |
I |
イソロイシン |
80 |
0 |
0 |
4.5 |
5.2 |
-1.70 |
中性 |
非極性(疎水性) |
Aliphatic |
6.02 |
| Leu |
L |
ロイシン |
70 |
0 |
0 |
3.8 |
4.9 |
-1.52 |
中性 |
非極性(疎水性) |
Aliphatic |
5.98 |
| Val |
V |
バリン |
50 |
0 |
0 |
4.2 |
5.9 |
-2.26 |
中性 |
非極性(疎水性) |
Aliphatic |
5.96 |
| Ala |
A |
アラニン |
20 |
0 |
0 |
1.8 |
8.1 |
-2.85 |
中性 |
非極性(疎水性) |
Aliphatic |
6.00 |
| Phe |
F |
フェニルアラニン |
140 |
15 |
0.107 |
2.8 |
5.2 |
-1.38 |
中性 |
非極性(疎水性) |
Aromatic |
5.48 |
| Pro |
P |
プロリン |
60 |
10 |
0.167 |
-1.6 |
8.0 |
-2.54 |
中性 |
非極性(疎水性) |
Pro & Gly |
6.30 |
| Met |
M |
メチオニン |
100 |
20 |
0.200 |
1.9 |
5.7 |
-1.87 |
中性 |
非極性(疎水性) |
Aliphatic |
5.74 |
| Cys |
C |
システイン |
60 |
20 |
0.333 |
2.5 |
5.5 |
-2.49 |
中性 |
極性(中性) |
Cysteine |
5.07 |
| Trp |
W |
トリプトファン |
180 |
130 |
0.722 |
-0.9 |
5.4 |
-1.05 |
中性 |
非極性(疎水性) |
Aromatic |
5.89 |
| Tyr |
Y |
チロシン |
140 |
115 |
0.821 |
-1.3 |
6.2 |
-2.26 |
中性 |
極性(中性) |
Aromatic |
5.66 |
| Lys |
K |
リシン |
80 |
70 |
0.875 |
-3.9 |
11.3 |
-3.05 |
塩基性 |
極性(塩基性) |
Positive |
9.74 |
| Gly |
G |
グリシン |
0 |
0 |
− |
-0.4 |
9.0 |
-3.21 |
中性 |
非極性(疎水性) |
Pro & Gly |
5.97 |
| His |
H |
ヒスチジン |
80 |
152 |
1.900 |
-3.2 |
10.4 |
-3.32 |
塩基性 |
極性(塩基性) |
Positive |
7.59 |
| Arg |
R |
アルギニン |
80 |
190 |
2.375 |
-4.5 |
10.5 |
-4.20 |
塩基性 |
極性(塩基性) |
Positive |
10.76 |
| Thr |
T |
トレオニン |
40 |
100 |
2.500 |
-0.7 |
8.6 |
-2.94 |
中性 |
極性(中性) |
Neutral |
6.16 |
| Glu |
E |
グルタミン酸 |
60 |
150 |
2.500 |
-3.5 |
12.3 |
-3.69 |
酸性 |
極性(酸性) |
Negative |
3.22 |
| Gln |
Q |
グルタミン |
60 |
200 |
3.333 |
-3.5 |
10.5 |
-3.64 |
中性 |
極性(中性) |
Neutral |
5.65 |
| Asp |
D |
アスパラギン酸 |
40 |
150 |
3.750 |
-3.5 |
13.0 |
-3.89 |
酸性 |
極性(酸性) |
Negative |
2.77 |
| Ser |
S |
セリン |
20 |
100 |
5.000 |
-0.8 |
9.2 |
-3.07 |
中性 |
極性(中性) |
Neutral |
5.68 |
| Asn |
N |
アスパラギン |
40 |
200 |
5.000 |
-3.5 |
11.6 |
-3.82 |
中性 |
極性(中性) |
Neutral |
5.41 |
※疎水性インデックスは以下を参照;Kyte and Doolittle, J. Mol. Biol., 157, 105-132(1982)
※log PはOn-Line Log P Calculation*掲載の実験値(参考ページ)
※極性・非極性はChimeのProtein選択様式と関連(参考ページ*)
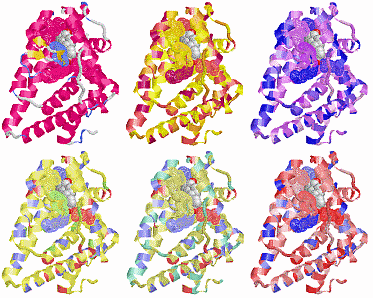
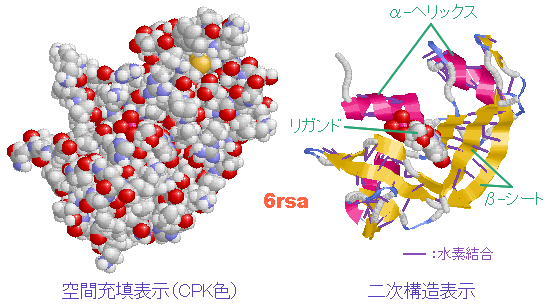
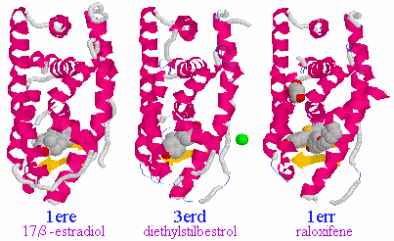
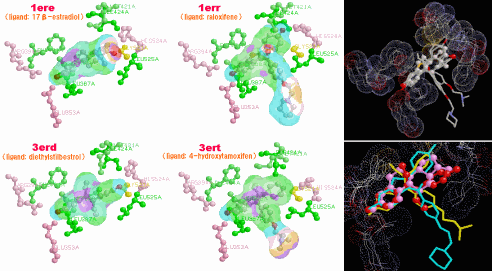
表1のアミノ酸の親水性・疎水性等によるタンパク質の色分け例(エストロゲン受容体1ereのChain A)
《上》左から,二次構造(後述),疎水性インデックス順,log P値順表示
《下》左から, 酸性・中性〈芳香族〉・塩基性アミノ酸区別,極性・非極性区別,表示.等電点順表示
※PDBコード順データリスト #,PDBデータのLigand結合部位 # などで各表示可能
※任意のPDBデータについて同様の表示をするにはPDBデータを詳細に見るために # を参照